
Nature Communications:科学家从深海微生物中发现并利用生物合成技术获得强效抗结核抗生素
近日, Nature Communications发表中科院南海海洋研究所热带海洋生物资源与生态重点实验室,中科院广州生物医药健康研究院呼吸疾病国家重点实验室,和广东医科大学合作的研究论文“Biosynthesis of ilamycins featuring unusual building blocks and engineered production of enhanced anti-tuberculosis agents. Nat. Commun. 2017, 8, 391, doi: 10.1038/s41467-017-00419-5”,报道了从深海放线菌中发现了具有抗结核杆菌系列活性物质,通过生物合成技术优化改造获得低细胞毒活性、强抗结核杆菌活性的化合物怡莱霉素 E。
结核病依然是最为严重的传染性疾病,其所引起的死亡率已经超过了HIV,位居传染性疾病之首。据WHO结核病年报报道,全球2015年新增结核病人1040万人,其中死亡约180万人。但是,目前临床上应用的4个一线抗结核药物和8个二线抗结核药物均是发现于上世纪的40年代到70年代期间,此后40年无新的抗结核药物出现。直至2012和2014年,FDA和欧盟先后分别批准了贝达喹啉(Bedaquiline)和Delamanid与其他抗结核药物联合使用治疗多重耐药结核杆菌的感染,但这两个药物依然存在副作用严重并且价格昂贵问题,临床应用受到一定限制。当前,多重耐药和泛耐药或全耐药结核菌株在迅速增长,加上结核病与HIV并发感染等情况的出现,给当前本已严峻的结核病防控形势带来了新的挑战,因此对高效低毒的新型抗结核药的需求日益迫切。
海洋中蕴藏着丰富的海洋微生物资源,其代谢产物尚未被充分发掘利用。深海环境营养匮乏,生活在深海的微生物为了争夺生存空间,会产生抗生素抑制周边微生物的生长。研究人员利用这一化学生态学原理从深海微生物中筛选抗菌活性物质。经过筛选,他们发现一株深海(-3560米)来源的放线菌发酵提取物对抗耻垢分枝杆菌具有较强的选择性抑制活性,并对肿瘤细胞增值具有一定的抑制活性。研究人员对菌株进行扩大培养和活性追踪分离,利用多种波谱技术解析了6个命名为怡莱霉素的活性物质结构(图1, 化合物1-6),并用单晶衍射技术测定了3个化合物的绝对构型。怡莱霉素属于环七肽类化合物,结构中含有独特的l-2-氨基-4-己烯酸,3-硝基-l-酪氨酸,和异戊烯基化的色氨酸结构单元;其中, l-2-氨基-4-己烯酸结构单元在其它天然产物中未见报道。此外,怡莱霉素结构中的亮氨酸结构单元和异戊烯基均被氧化。
科研人员随后阐明了怡莱霉素的生物合成机制,并利用生物工程技术构建突变株,期望构建新结构衍生物,简化代谢产物组分,并提高目标组分的产量。科研人员对怡莱霉素产生菌进行了基因组测序,根据怡莱霉素的结构特征,通过生物信息分析和基因敲除技术,确定了负责怡莱霉素的生物合成基因簇(图1,a)和骨架结构的生物合成过程(图1,b)。对四个功能基因进行敲除和代谢产物分析,结合前体分子喂养及同位素标记实验,阐明了新颖的I型聚酮合酶 IlaE、细胞色素P450氧化酶IlaD、氨基转移酶IlaH和II型硫酯酶IlaF负责稀有结构单元l-2-氨基-4-己烯酸的生物合成(图1,e)。对怡莱霉素生物合成基因簇中的一氧化氮合酶IlaM和细胞色素P450氧化酶IlaN所编码的基因进行敲除和代谢产物分析,及前体分子回补实验,阐明了L-酪氨酸的硝基化过程(图1,d)。通过对怡莱霉素生物合成基因簇中的异戊烯基转移酶IlaO和另外两个细胞色素P450(IlaL和IlaR)所编码的基因进行敲除,代谢产物分析,以及中间体的分离和结构鉴定,阐明了IlaO在怡莱霉素形成过程中负责色氨酸的异物烯基化的前修饰作用(图1,c),IlaL和IlaR这两个酶在怡莱霉素生物合成过程中分别负责亮氨酸末端甲基的羧基化及异物烯基的环氧化的后修饰(图1,f)。通过上述研究,科研人员精细阐明了怡莱霉素生物合成过程中的三个前修饰和两个后修饰过程,并得构建了高产菌株,定向生产新结构 衍生物怡莱霉素E和F。
衍生物怡莱霉素E和F。
最后,科研人员系统评价了分离和工程改造获得的系列怡莱霉素衍生物对结核分枝杆菌M. TuberculosisH37Rv,5种人体肿瘤细胞株和2种正常细胞株的抑制活性,研究结果发现怡莱霉素E的体外抗结核活性为9.8 nM,是一线抗结核药物利福平活性的30倍,怡莱霉素E对乳腺癌等肿瘤细胞也显示一定抑制活性,对正常细胞的毒性较低,在抗结核活性和细胞毒性之间的选择性指数为400-1500,显示出较好的安全性窗口,具有成药潜力(发明专利申请号:20160906737.1,201610805549.7,201610885104.4)。该研究发现并阐明了海洋微生物复杂活性代谢产物怡莱霉素的生物合成机制,并且获得了具有更好活性和低毒性的抗结核活性化合物,为新型抗结核药物的进一步开发提供了化学实体。
中科院南海海洋所的马俊英副研究员为论文的第一作者和共同通讯作者,鞠建华研究员为论文的共同通讯作者,中科院广州生物医药与健康研究院呼吸疾病国家重点实验室的张天宇研究员和广东医科大学的张华副教授分别测试化合物的抗结核活性和细胞毒活性。研究工作得到了国家自然科学基金、中国科学院、广东省自然科学基金团队和广州市科技计划项目的资助。
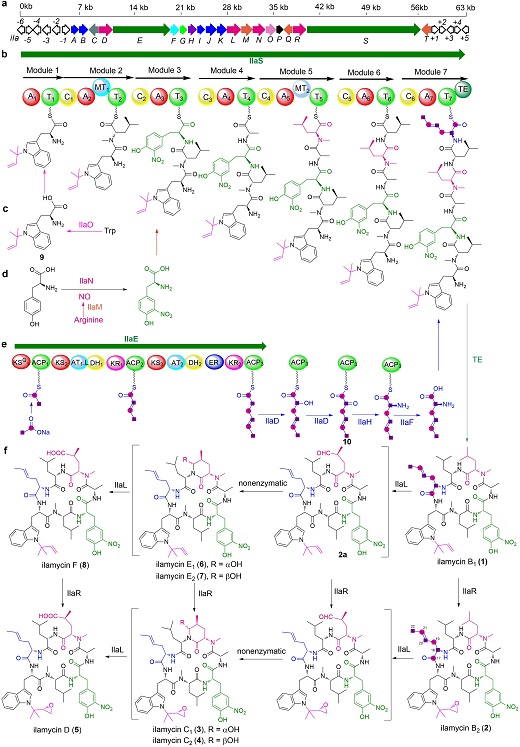
图1, 怡莱霉素的生物合成基因簇及其生物合成过程。a) 怡莱霉素的生物合成基因簇;b)怡莱霉素的骨架结构的合成过程;c) 色氨酸的异戊烯基化过程;d)酪氨酸的硝基化过程; e) L-2-氨基-4-己烯酸的生物合成机制;f) 怡莱霉素的氧化后修饰过程。
附件下载: